临床试验项目结题工作指引
作者: 湛江中心人民医院 来源: 湛江中心人民医院 编辑: 湛江中心人民医院 发布时间: 2026-03-09 点击数: 49
临床试验项目结题工作指引
为保证结题工作质量,提高结题工作效率,特制订本指引,请申办者/CRO遵照执行。
一、临床试验结题流程
1. 所有受试者完成出组随访后,监查员下载附件1《合同费用结算表》,与机构项目管理员联系导出受试者检查费、补助费用,结余费用实行多退少补,申办方/CRO完成尾款结算,在CTMS系统上传尾款打款凭证并提交开票申请,CTMS流程详见通知公告《开发票工作指引》。
2. 临床试验经费结算完成后,监查员填写附件2《临床试验小结表》与系统申请伦理结题审查(系统申请具体操作流程详见:三、CTMS系统伦理结题申请操作流程)。
3. 准备临床试验用药物/器械退还、归档资料整理等工作。
4. 填写附件3《临床试验结题申请表》
① 伦理委员会完成结题审查,伦理办完成签字盖章。
② 监查员与机构GCP药物管理员、器械管理员联系完成试验用药品/医疗器械退还工作,审核签字。
③ 监查员与科室资料管理员完成研究者文件交接工作,资料管理员确认无误后签核签字。
④ 主要研究者、专业组负责人审核签字。
⑤ 机构档案管理员检查归档资料完整性,审核签字。
⑥ 项目管理员确认完成临床试验经费结算,审核签字。
⑦ 机构办主任完成审核签字。
二、系统递交结题申请
1.选择结题申请、选择对应的项目
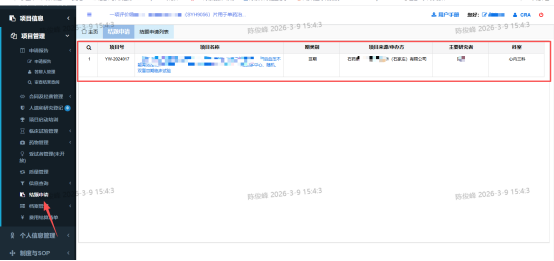
2.选择新增、上传对应的文件(小结表、结题申请表、结算表等文件)
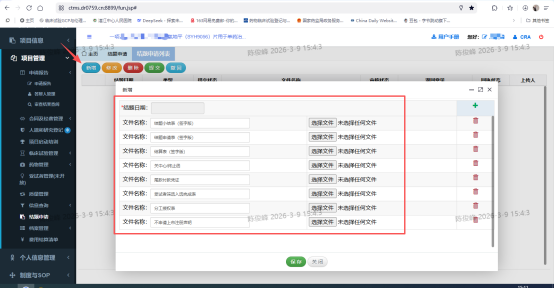
3.选择并提交结题申请。
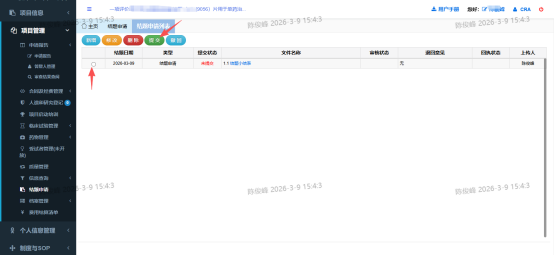
三、CTMS系统伦理结题申请操作流程
1.新增报告类型,选择研究完成报告
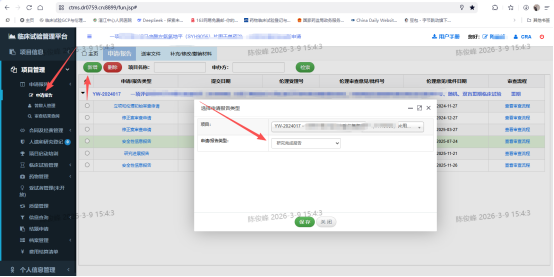
2.填写研究完成报告
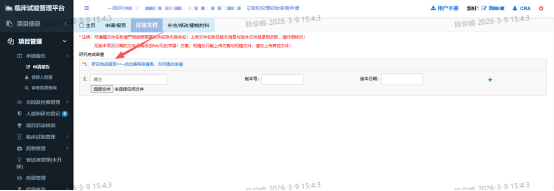
四、注意事项
(一)CRA必须在整理完所有原始数据及锁库前通知机构进行结题质控/稽查。
(二)分中心小结可采用机构模板和申办方模板。
(三)分中心小结盖章前需要完成质控反馈、尾款支付。
(四)已召开中心启动会的项目,关闭中心时即使项目未进行筛选,仍需归档项目资料。项目产生的药物管理费、文件管理费等费用不予退还。
(五)EDC锁库后3个月内提交项目资料到机构办归档。
地址:广东省湛江市赤坎区源珠路236号(南门)、广东省湛江市赤坎区康宁路(北门)
医院电话:0759—3157999
邮编:524045
医院网址:www.dr0759.cn
版权所有:广东省湛江中心人民医院 Copyright 2008 dr0759.cn All Rights Reserved.网站备案号:粤ICP备11087513号