临床试验SAE/SUSAR/DSUR报告工作流程
作者: 湛江中心人民医院 来源: 湛江中心人民医院 编辑: 湛江中心人民医院 发布时间: 2026-03-04 点击数: 250
临床试验SAE/SUSAR/DSUR报告工作流程
为规范我院临床试验中安全性信息的报告流程,特制定本工作流程,请各方遵照执行。
规程:
一、SAE上报
1. SAE定义
严重不良事件(SAE,Serious Adverse Event)指受试者接受试验用药品后出现死亡、危及生命、永久或者严重的残疾或者功能丧失、受试者需要住院治疗或者延长住院时间,以及先天性异常或者出生缺陷等不良医学事件。
医疗器械临床试验过程中发生的导致死亡或者健康状况严重恶化,包括致命的疾病或者伤害、身体结构或者身体功能的永久性缺陷、需要住院治疗或者延长住院时间、需要采取医疗措施以避免对身体结构或者身体功能造成永久性缺陷;导致胎儿窘迫、胎儿死亡或者先天性异常、先天缺损等事件。
2. SAE报告流程
2.1报告时限:
(1)药物临床试验:研究者获知SAE 24小时内报告申办方、伦理委员会、机构办公室(研究方案或其他文件中如有其他特殊规定不需立即报告的SAE除外);随后应当及时提供详尽、书面的随访报告。
(2)医疗器械临床试验:研究者获知SAE24小时内向申办者、机构办公室、伦理委员会报告;并按照临床试验方案的规定随访严重不良事件,提交严重不良事件随访报告。
2.2本院SAE报告方式:
(1)报告申办方:研究者在获知受试者出现SAE 24 小时内及时通过邮件等方式报告申办方,SAE 报告模版可使用申办方模版/机构模版/国家局发布的模版。
(2)报告机构办公室和伦理委员会:研究者在获知受试者出现 SAE 24 小时内通过CTMS管理系统上报机构和伦理,受理后递交书面报告至机构办公室与伦理办公室(两种方式均须实施),系统上报具体操作流程详见:四、CTMS管理系统上报机构办公室操作流程。
CTMS管理系统:https://ctms.dr0759.cn:8899/fun.jsp#
备注:机构/伦理仅通过CTMS系统线上接收安全性事件,不接受邮件等其他形式上报
二、SUSAR上报
1. SUSAR的定义
SUSAR(suspect unexpected serious adverse reaction)可疑且非预期严重不良反应:指临床表现的性质和严重程度超出了试验药物研究者手册、已上市药品的说明书或者产品特性摘要等已有资料信息的可疑并且非预期的严重不良反应。
2.SUSAR报告流程
2.1报告时限:
(1)对于致死或危及生命的SUSAR:申办方应在首次获知7天内尽快报告,并在随后的8天内报告、完善随访信息。(申办者首次获知当天为第0天)
(2)对于非致死或危及生命的SUSAR:申办者应在首次获知后尽快报告,但不得超过15天。
(3)对于非本中心SUSAR报告递交,申办者应定期汇总备案,通常为季度报告,至少每3个月汇总报告一次。
2.2本院SUSAR报告方式:
(1)报告研究者:申办方收到SAE报告后判定为SUSAR的情况下,申办方应在法规要求的时限内(时限详见2.1)将判定依据以电子版形式和书面形式递交主要研究者或授权研究者,根据申办方提供的SUSAR报告,主要研究者或授权研究者应衡量继续开展试验的风险和获益,如研究参与者继续参与试验的风险/获益比明显增高,应考虑采取及时和恰当的措施保护在研究参与者安全和权益,并应当向伦理委员会报告由申办方提供的可疑且非预期严重不良反应。
(2)报告机构办公室和伦理:申办方收到SAE报告后判定为SUSAR的情况下申办方应在法规要求的时限内(时限详见2.1)将判定依据通过CTMS管理系统上报机构和伦理,受理后递交书面报告至机构办公室与伦理办公室(两种方式均须实施),系统上报具体操作流程详见:四、CTMS管理系统上报机构办公室操作流程。CTMS管理系统:https://ctms.dr0759.cn:8899/fun.jsp#
备注:机构/伦理仅通过CTMS系统线上接收安全性事件,不接受邮件等其他
形式上报
2.3外院SUSAR报告方式:
申办者收到外院SUSAR后,应通过CTMS管理系统上报机构和伦理,受理后递交书面报告至机构办公室与伦理办公室(两种方式均须实施),以汇总报告的形式(如总体安全性评估和行列表)定期提交,但原则上不得超过3个月(以申办者获知事件为0天计算)。
三、DSUR的报告
关于研发期间安全性更新(DSUR)报告,应当参照ICH-E2F及CDE发布的《研发期间安全性更新报告要求及管理规定》进行年度报告,由申办者收集、定期递交主要研究者或授权研究者审阅、签字后,分别递交至临床试验机构审核、伦理委员会审查,并上报药监部门、卫健委,原则上报告周期不超过一年;系统上报具体操作流程详见:四、CTMS管理系统上报机构办公室操作流程。CTMS管理系统:https://ctms.dr0759.cn:8899/fun.jsp#
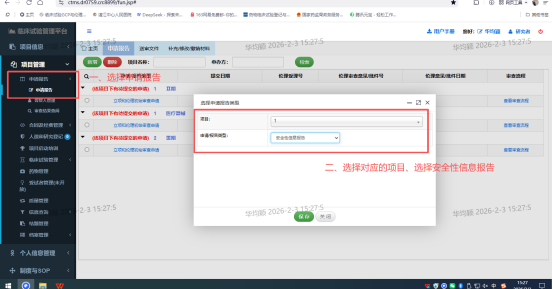
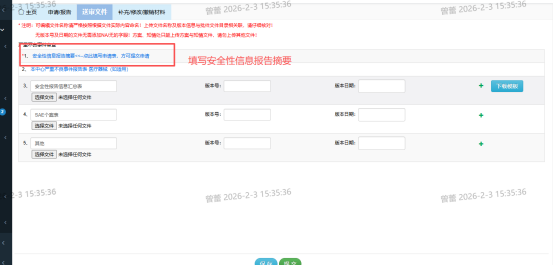
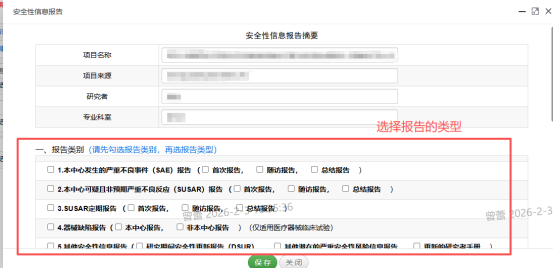
四、CTMS管理系统上报机构办公室/伦理操作流程:
地址:广东省湛江市赤坎区源珠路236号(南门)、广东省湛江市赤坎区康宁路(北门)
医院电话:0759—3157999
邮编:524045
医院网址:www.dr0759.cn
版权所有:广东省湛江中心人民医院 Copyright 2008 dr0759.cn All Rights Reserved.网站备案号:粤ICP备11087513号